肝癌惡性腹水(MA)是臨床治療難題,現有化療手段受限于腫瘤靶向性差和免疫抑制微環境,療效有限且副作用明顯。
近日,澳門科技大學中醫藥學院徐渴陽助理教授團隊,聯合中國中醫科學院中醫基礎理論研究所楊玉琴、蔡夢如助理研究員、北京中醫藥大學褚福浩副教授,基於傳統中藥「芫花-甘草」配伍啓發,通過「一鍋法」綠色合成,成功研發出新型可注射多組分中藥水凝膠(GK-GA)。研究團隊以芫花(Genkwa Flos, GK)乙酸乙酯活性提取物爲原料,僅添加單一藥用輔料甘草酸(GA),在溫和條件下自組裝而成,兼具優异的可注射性與腹腔長效滯留特性。
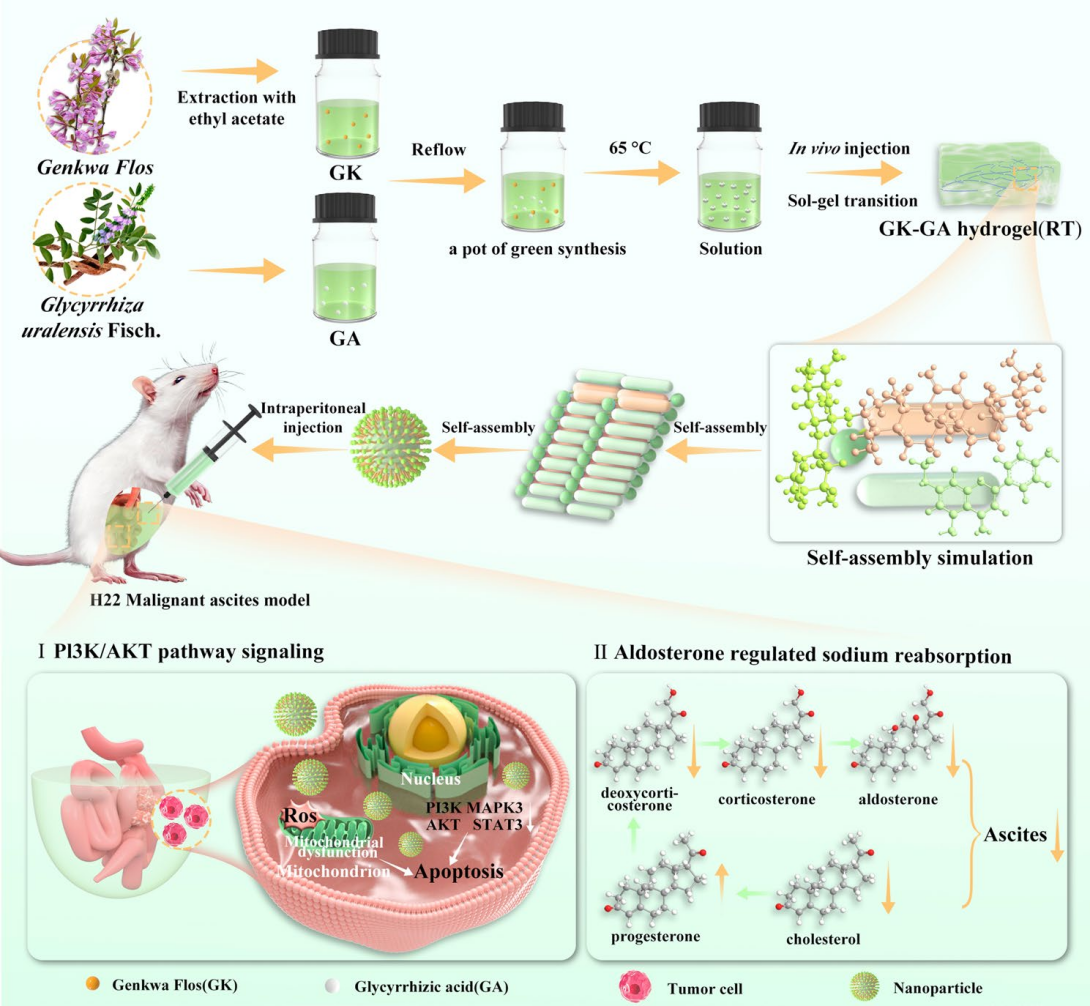
GK-GA可注射多組分中藥水凝膠治療肝癌惡性腹水的機制示意圖
該研究實現了「雙管齊下」的雙重療效:
一是「以毒攻毒」:作爲促雕亡劑,顯著提升H22肝癌細胞內ROS水平,導致綫粒體膜電位去極化,下調PI3K-AKT及JAK2/STAT3信號通路關鍵蛋白(MAPK3、SRC等),使細胞雕亡率從對照組的3.32%升高至23.15%,同時展現出優于單獨芫花或甘草酸的細胞攝取能力;
二是「疏堵結合」:作爲代謝調節劑,精準幹預醛固酮合成與分泌及醛固酮調節的鈉重吸收通路,顯著下調膽固醇、脫氧皮質酮、皮質酮、醛固酮,上調孕酮,從源頭抑制腹水生成。
團隊在體外成功驗證了GK-GA的細胞毒性(CCK-8法)、ROS升高、綫粒體功能障礙及雕亡誘導(Annexin V-FITC/PI染色);在H22肝癌腹水小鼠模型中,腹腔注射GK-GA(6.25 mg/kg)後,腹水生成量較模型組減少47.62%,小鼠體重與腹圍顯著改善;活體熒光成像(Cy7標記)證實其在腹腔、肝、腎的滯留時間遠長于游離藥物;主要器官(肝、心、脾、肺、腎、回腸、結腸)病理檢查未見明顯毒性,具備良好的生物相容性與安全性。
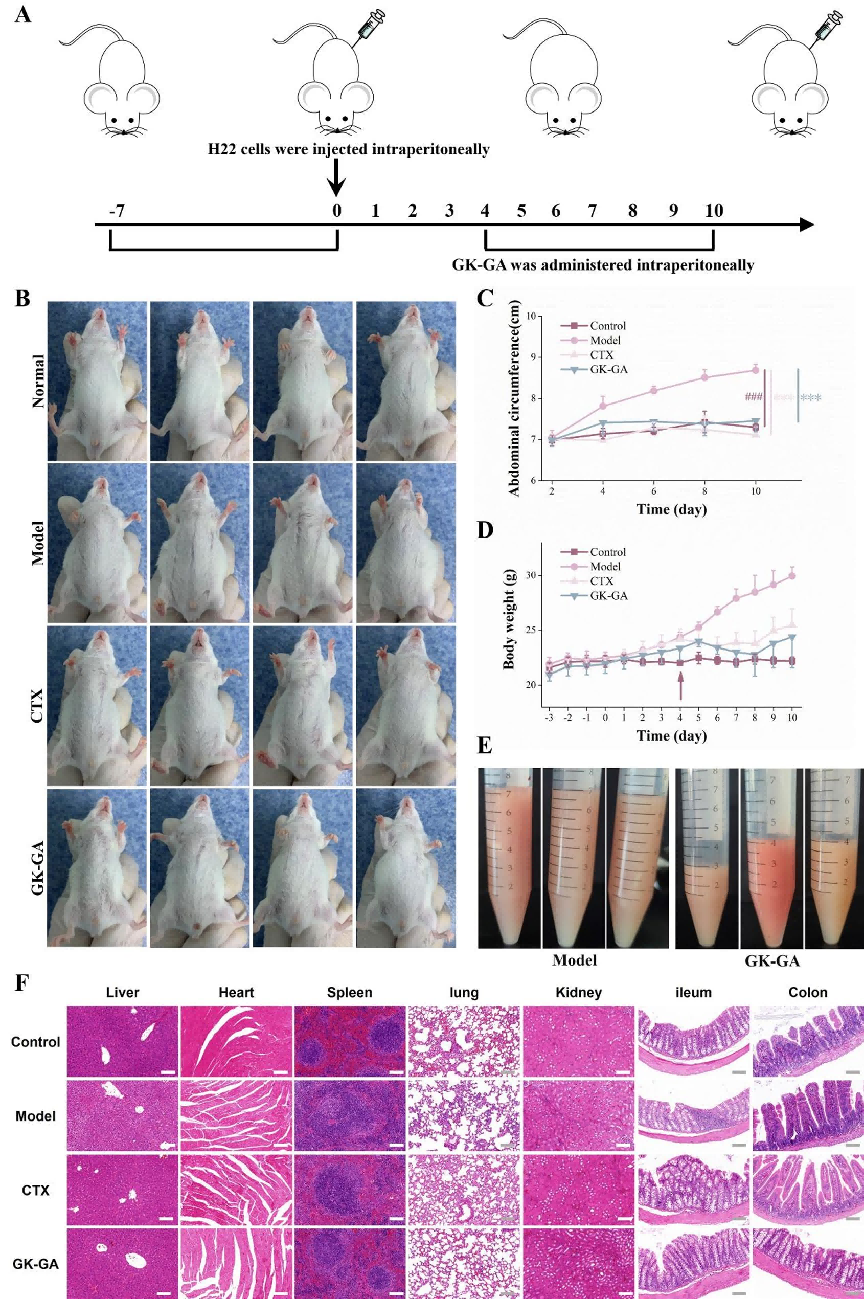
GK-GA腹腔注射後腹水量較模型組减少47.62%
這項成果不僅爲肝癌惡性腹水治療提供了低毒高效的腹腔給藥新策略,更展示了「中藥有效部位自組裝+多組學」(網絡藥理學、轉錄組學、非靶向/靶向代謝組學)技術在現代醫學中的巨大潜力,爲中醫「多成分、多通路、多靶點」整體治療理念的現代化提供了全新平臺型技術與普適性新思路。
上述成果以“Injectable multi-component hydrogels for the treatment of ascites caused by hepatocellular carcinoma via anti-tumor and reduction of ascites generation”爲題,發表于Springer Nature出版集團旗下納米生物技術領域頂刊Journal of Nanobiotechnology(IF=12.6,在納米科學與納米技術領域位居全球前2.3%)。澳門科技大學徐渴陽助理教授為共同通訊作者之一,論文共同第一作者為中國中醫科學院基礎理論研究所助理研究員楊玉琴、北京中醫藥大學研究生亓金釵,郎英琦。





